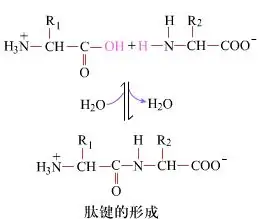
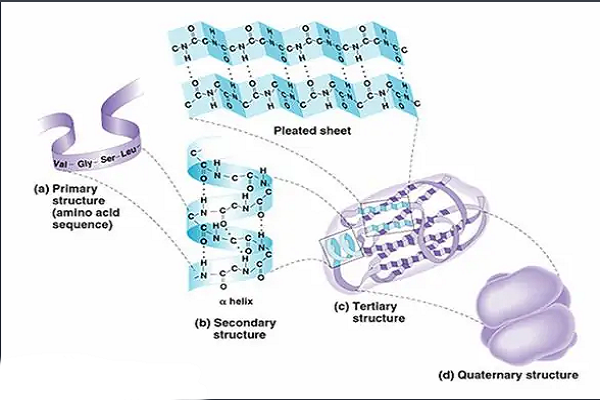
表面上では、ジペプチドを生成するペプチド結合の形成は単純な化学プロセスです。これは、2つのアミノ酸成分が脱水された状態でペプチド結合、アミド結合によって結合していることを意味します。
ペプチド結合の形成は、穏やかな反応条件下でのアミノ酸の活性化です。(A) カルボキシル部分、2 番目のアミノ酸 (B) 求核的に活性化されたカルボキシル部分は、ジペプチド (AB) を形成します。「(A)のカルボキシル成分が保護されていないと、ペプチド結合の形成を制御することができません。」直鎖状および環状ペプチドなどの副産物が標的化合物 AB と混合される場合があります。したがって、ペプチド結合形成に関与しないすべての官能基は、ペプチド合成中に一時的に可逆的な方法で保護されなければなりません。
したがって、ペプチド合成、つまり各ペプチド結合の形成には、3 つの凝集ステップが含まれます。
最初のステップは、保護が必要なアミノ酸を準備することですが、アミノ酸の両性イオン構造はもはや存在しません。
第 2 ステップは、ペプチド結合を形成するための 2 段階の反応で、最初に N-保護アミノ酸のカルボキシル基が活性化されて活性中間体となり、次にペプチド結合が形成されます。この連動反応は、1 段階の反応として、または 2 つの連続した反応として発生します。
第三のステップは、保護ベースの選択的除去または完全な除去です。すべての除去はすべてのペプチド鎖が組み立てられた後にのみ行うことができますが、ペプチド合成を続行するには保護基の選択的な除去も必要です。
10 個のアミノ酸 (Ser、Thr、Tyr、Asp、Glu、Lys、Arg、His、Sec、Cys) には選択的保護が必要な側鎖官能基が含まれているため、ペプチド合成がより複雑になります。一時的保護基地と半永久的保護基地は、選択性の要件が異なるため、区別する必要があります。一時的な保護基は、アミノ酸またはカルボキシル官能基の一時的な保護を反映するために次のステップで使用されます。半永久的な保護基は、場合によっては合成中に、既に形成されたペプチド結合やアミノ酸側鎖を妨げることなく除去されます。
「理想的には、カルボキシル成分の活性化とその後のペプチド結合の形成(カップリング反応)は、ラセミ体や副生成物の形成なしに迅速に行われ、高収率を達成するにはモル反応物を適用する必要があります。」残念ながら、これらの要件を満たす化学カップリング方法はなく、実際の合成に適したものはほとんどありません。
ペプチド合成中、さまざまな反応に関与する官能基は通常、手動中心にリンクされますが、グリシンは唯一の例外であり、回転の潜在的なリスクがあります。
ペプチド合成サイクルの最終ステップは、すべての保護基の除去です。保護基の選択的除去は、ジペプチド合成における保護の完全な除去の要件に加えて、ペプチド鎖の伸長にも重要です。合成戦略は慎重に計画する必要があります。戦略的な選択に応じて、N はα-アミノまたはカルボキシル保護基を選択的に除去できます。「戦略」という用語は、個々のアミノ酸の縮合反応の順序を指します。一般に、段階的合成とフラグメント凝縮の間には違いがあります。ペプチド合成 (「従来の合成」とも呼ばれます) は溶液中で行われます。ほとんどの場合、ペプチド鎖を徐々に長くするには、ペプチド鎖を使用してより短いフラグメントを合成する必要があります。より長いペプチドを合成するには、標的分子を適切なフラグメントに分割し、C 末端での分化の程度を最小限に抑えることができることを確認する必要があります。個々のフラグメントが徐々に組み立てられた後、目的の化合物が結合されます。ペプチド合成の戦略には、最良かつ最も適切な保護フラグメントの選択が含まれ、ペプチド合成の戦略には、保護塩基の最も適切な組み合わせとフラグメント結合の最適な方法の選択が含まれます。
投稿日時: 2023 年 7 月 19 日