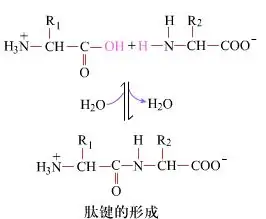
表面上、ペプチド結合の形成はジペプチドを生成し、単純な化学プロセスです。これは、2つのアミノ酸成分が、脱水状態である間、ペプチド結合、アミド結合によってリンクされていることを意味します。
ペプチド結合形成は、軽度の反応条件下でのアミノ酸の活性化です。 (A)カルボキシル部分、2番目のアミノ酸(B)結核性活性化カルボキシル部分がジペプチド(A-B)を形成します。 「カルボキシル成分(a)が保護されていない場合、ペプチド結合の形成を制御できません。」線形および環状ペプチドなどの副産物は、標的化合物A-Bと混合できます。したがって、ペプチド結合の形成に関与しないすべての官能基は、ペプチド合成中に一時的に可逆的に保護する必要があります。
したがって、ペプチド合成 - 各ペプチド結合の形成 - には、3つのステップの凝集が含まれます。
最初のステップは、保護を必要とするいくつかのアミノ酸を調製することであり、アミノ酸のZwitherionic構造はもはや存在しません。
2番目のステップは、ペプチド結合を形成するための2段階の反応であり、Nで保護されたアミノ酸のカルボキシル基が最初に活性中間体に活性化され、次にペプチド結合が形成されます。この結合反応は、ワンステップ反応として、または2つの連続反応として発生する可能性があります。
3番目のステップは、保護ベースの選択的除去または完全な除去です。すべての除去は、すべてのペプチド鎖が組み立てられた後にのみ発生しますが、ペプチド合成を継続するためには、保護基の選択的除去も必要です。
10個のアミノ酸(Ser、Thr、Tyr、Asp、Glu、Lys、Arg、His、Sec、およびCys)には、選択的保護が必要なサイドチェーン機能グループが含まれているため、ペプチド合成をより複雑にします。選択性の要件が異なるため、一時的な保護および半多数の保護ベースを区別する必要があります。一時的な保護グループは、アミノ酸またはカルボキシル官能基の一時的な保護を反映するために、次のステップで使用されます。合成中に、既に形成されたペプチド結合またはアミノ酸側鎖を干渉することなく、半多数の保護グループが除去されます。
「理想的には、カルボキシル成分の活性化とその後のペプチド結合の形成(結合反応)は、ラセミまたは副産物の形成なしでは迅速でなければならず、モル反応物を適用して高収量を達成する必要があります。」残念ながら、化学カップリング方法はこれらの要件を満たすものではなく、実用的な統合に適したものはほとんどありません。
ペプチド合成中、さまざまな反応に関与する官能基は通常、マニュアルセンターにリンクされており、グリシンが唯一の例外であり、回転の潜在的なリスクがあります。
ペプチド合成サイクルの最後のステップは、すべての保護グループの除去です。ジペプチド合成における保護を完全に除去するための要件に加えて、保護基の選択的除去はペプチド鎖伸展にとって重要です。合成戦略は慎重に計画する必要があります。戦略的な選択に応じて、Nはα-アミノまたはカルボキシル保護基を選択的に除去できます。 「戦略」という用語は、個々のアミノ酸の一連の凝縮反応を指します。一般に、漸進的な合成とフラグメント凝縮には違いがあります。ペプチド合成(「従来の合成」とも呼ばれる)は、溶液中に行われます。ほとんどの場合、ペプチド鎖の段階的延長は、ペプチド鎖を使用して短い断片を合成することによってのみ合成できます。より長いペプチドを合成するには、標的分子を適切な断片に分割し、C末端での分化の程度を最小限に抑えることができると判断する必要があります。個々のフラグメントが徐々に組み立てられた後、ターゲット化合物が結合されます。ペプチド合成の戦略には、最良かつ最も適切な保護断片の選択が含まれ、ペプチド合成の戦略には、保護塩基の最も適切な組み合わせの選択と断片的抱合の最良の方法が含まれます。
投稿時間:2025-07-02